ПРИЛОЖЕНИЕ № 2
![]()
Тема. Вода в природе. Понятие о
растворах. Свойства воды. Применение, очистка
воды.
Цель урока. Знакомство учащихся с
особенностями воды как ценного природного
вещества.
Тип урока: получение новых знаний.
Доминирующий метод: объяснительно-иллюстративный.
Формы организации учебной деятельности: фронтальная.
Оборудование: глобус, схема "Вода", растворы и оборудование для проведения опытов, рельефные таблицы "Овраг", "Пещера", динамическое пособие "Круговорот воды в природе", Дистиллятор, схема городской водоочистной станции.
Ход урока.
Люди издавна уделяли большое
внимание воде, поскольку было хорошо известно,
что там, где нет воды, нет и жизни.
Посмотрите на глобус, и вы увидите, что
поверхность земного шара на 3/4 покрыта водой - это
океаны, моря, озера, ледники. Общие запасы
свободной воды на Земле составляют 1,4 млр.км.
По таблице рассмотреть
распределение воды на Земле.
2. Круговорот воды в природе.
Вопрос: Почему количество воды на Земле остается неизменным?
Вода находится в постоянном и
активном кругообороте. Его движущей силой
является Солнце, а основным источником воды -
Мировой океан. Почти четверть всей падающей на
Землю солнечной энергии расходуется на
испарение воды с поверхности водоемов. Примерно
2/3 атмосферной воды возвращается в виде осадков
обратно в океан, а 1/3 выпадает на сушу. Эта вода
пополняет ледники, реки и озера. В свою очередь
материковые поверхностные воды снова стекают в
моря и океаны, растворяя встречающиеся им на пути
породы (демонстрация рельефной таблицы
"Пещера", "Овраг").
Увлажняющая почву вода всасывается
корнями растений. Вместе с водой растения
получают растворенные питательные вещества. В
растениях она поднимается по стеблям и
возвращается в виде пара в атмосферу через
листья. Важным регулятором воды на суше являются
горные ледники. Они отдают воду в основном в
летние месяцы.
С круговоротом воды происходит
перемещение тепла.
Объяснение ведется одновременно с
построением этапов круговорота воды с
использованием динамического пособия
"Круговорот воды в природе".
Демонстрация: Испарение воды и конденсации пара (см.рис. 1)
Обороудование: колба с водой, химический стакан, пробка с газоотводной трубкой, спиртовка, спички, стекло, 2 металлических штатива.
3. Физические свойства воды.
Работа по схеме "Вода".
Вода - жидкость без вкуса, цвета,
запаха, t кип.=100С, Тпл=0 С. р=1г/см .
Вопрос: В каких состояниях может
находиться вода? Приведите примеры.
Единственное вещество в природе,
которое в земных условиях существует во всех
трех агрегатных состояниях: жидком (вода),
твердом (лед), газообразном (пар).
4. Вода - растворитель.
Вода в природе всегда раствор. В воде
рек солей мало, поэтому она пресная, а в воде
морей и океанов солей много, поэтому она
горько-соленая. Растворы - прозрачны.
В природной воде, кроме солей, могут
быть даже различные нерастворимые частицы,
которые делают ее мутной. Мутная вода - это взвесь
(смесь чистой воды и примесей).
В народе говорят: "Вода камень
точит". Она разрушает даже гранит. Ручьи, реки,
потоки дождевой воды постоянно растворяют соли и
другие вещества минералов и горных пород. Эти
растворы попадают в моря и океаны.
Многие явления природы происходят
благодаря тому, что вода - хороший растворитель. В
живых организмах постоянно передвигаются
растворы. Сок растений, кровь животных - это и
растворы и взвеси одновременно. Они разносят
необходимые для жизни вещества по всему телу.
В воде хорошо растворяются многие
газы, жидкости и твердые вещества.
Процесс растворения сочетает в себе
физический процесс (дробление до молекул) и
химическое взаимодействие компонентов.
Вопрос: Какие растворы встречаются вам
в повседневной жизни? Каково применение этих
растворов?
Демонстрация занимательных опытов с комментариями.
Занимательные опыты. (необычные растворы)
Опыт 1. Минеральный хамелеон.
Как известно, хамелеоном называют
ящерицу, быстро изменяющую свою окраску под
влиянием окружающей среды. Сходным внешним
свойством обладают некоторые растворы. Нагреть
перманганат калия ![]()
Затем растворить полученную соль в воде, и
образуется раствор, который тут же переходит в
сине-фиолетовый, фиолетовый, малиновый.
![]()
Оборудование: спиртовка, спички, тв. ![]() ., стакан, вода.
., стакан, вода.
Опыт 2. Превращение "молока" в
воду.
К белому осадку, полученному сливанием
раствора хлорида кальция и карбоната натрия,
добавляют избыток раствора соляной кислоты.
Жидкость вскипает и становится бесцветной и
прозрачной.
Оборудование: р-ры ![]()
Опыт 3. Изменение окраски раствора.
Кусочек натрия бросают в широкий
цилиндр, заполненный до половины водой. Натрий
активно взаимодействует с водой, движется по
поверхности, шипит, достигая стенки сосуда,
искрит и полностью сгорает. Добавляют в цилиндр
несколько капель раствора фенолфталеина и
размешивают стеклянной палочкой. Жидкость
приобретает яркий малиновый цвет. Затем
приливают к жидкости немного любой кислоты.
Снова размешивают, раствор становится
прозрачным и бесцветным.
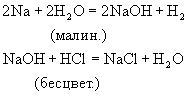
Оборудование: Na, цилиндр с водой, стекл.палочка, р-р фенолфталеина, р-р НСL.
Опыт 4. Дым без огня.
Стеклянные палочки смачивают одну в
конц. растворе НСL, а другую - в конц.р-ре NН ОН. При
сближении палочек появляется дым.
![]()
Оборудование:
![]()
5. Применение воды и ее очистка.
В быту, в различных промышленных
производствах, сельском хозяйстве широко
используется вода и водные растворы.
В засушливых районах планеты на
человека приходится 20 л воды в день, а больших
промышленных городах дневной расход превышает 200
л на каждого жителя (в Ярославле, например - 350 л).
В то же время отдельные производства
загрязняют реки и другие водоемы, делая
находящуюся там воду непригодной для жизни в ней
животных и для использования ее человеком. На
предприятиях строят специальные очистные
сооружения, предотвращающие попадание ядовитых
веществ в реки и озера. На некоторых заводах
использованную воду очищают и вновь направляют в
цеха. Так удается не только сократить расходы
пресной воды, но и сохранить чистыми близлежащие
от завода водоемы.
Для всех разнооборазных
потребностей человека нужна только пресная вода,
освобожденная от посторонних примесей.
Чтобы приготовить растворы в аптеках,
лабораториях, применяют дистиллированную воду,
получаемую при конденсации пара в специальных
аппаратах (демонстрация дистиллятора).
Вам хорошо известно, как и где
используют воду. К нам она поступает из
артезианской скважины из-под земли. Подземная
вода не нуждается в очистке.
В городах в водопровод вода поступает
из водохранилищ. Но предварительно эту воду
тщательно очищают. Сначала освобождают от песка
и глины в специальных отстойниках. Затем воду
обеззараживают хлором, озоном, чтобы убить в ней
болезнетворные микробы (см.рис.3).
6. Обобщение.